作者:天堂硅谷投资管理部
联系方式:anzheng@ttgg.com.cn
一、前言:血浆蛋白构成
人体血液共分为血浆(50%)、红细胞(42%)、白细胞和血小板(8%),其中血浆由水(90%)、糖类电解质(3%)和蛋白质(7%)组成。血液中不同的蛋白组分经分离提纯后可制成血液制品,针对不同病症的患者使用。血液制品是从7%的蛋白质中分离提纯制成的。
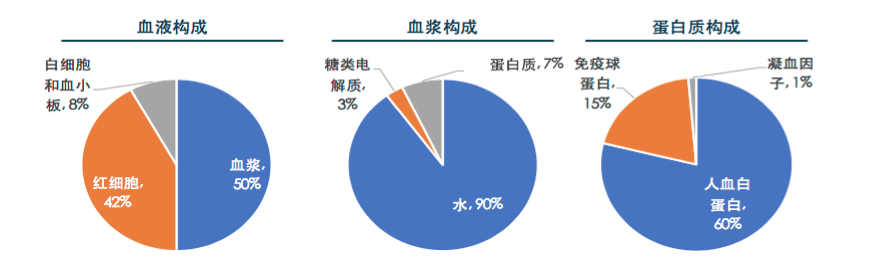
图表 1 - 血浆、血浆和血浆蛋白类别构成
血浆中的有效成本数量超过200种,可分离纯化超过100种,经常研究的约70种,国内临床的产品约20种。
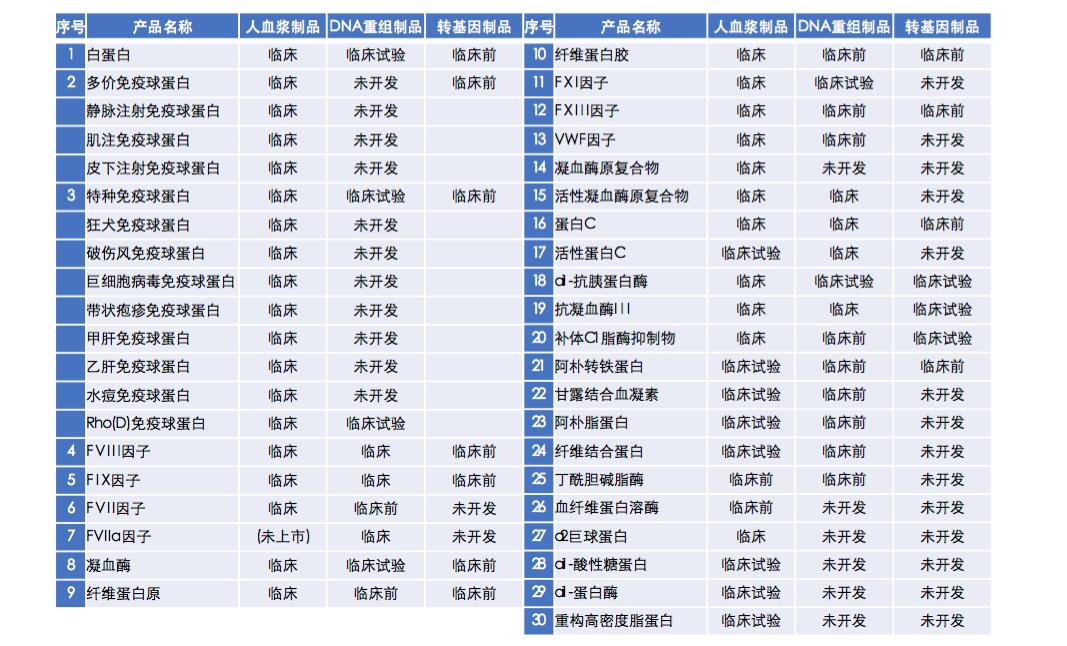
图表2 - 海外血浆蛋白开发情况
(弘则研究)
二、分离提纯工艺介绍
分离提纯是血制品的制备过程中的核心环节之一,利用不同血液组分之间性质差异,使用物理或化学手段将其彼此分离,形成可供治疗使用的产品。目前,血制品企业常用的生产工艺通常分为低温乙醇法和层析法两大类。
低温乙醇法(国元证券)
二战时期美国教授Cohn首创血浆蛋白纯化分离技术,被业界成为Cohn法。该方法通过对原料血浆的蛋白质浓度、pH值、乙醇浓度、离子强度、温度这5大参数的调整,逐级沉淀血浆,将血浆分为五个沉淀组分,血浆蛋白也按分子大小顺序先后分离至各组分中。二十世纪六十年代,瑞士的Nitschmann和Kistler教授对Cohn法进行改进,成功缩短了生产的周期同时提高了收率,形成Nitschmann-Kistler法。
层析法
层析法(Chromatography,又称色谱法)利用不同物质在不同相态的选择性分配,以“流动相”对“固定相”中的混合物进行洗脱,混合物中不同的物质会以不同的速度沿“固定相”移动,最终达到分离的效果。
层析法的构成十分丰富。根据层析床的形状,可分为柱层析(Column chromatography)和平面层析(Planar chromatography);根据流动相的物理性状,可以分为气体层析(Gas Chromatography)、液体层析(Liquid chromatography);根据分离机制,可以分为离子交换层析(Ion exchange chromatography)、扩张床层析(Expanded bed adsorption chromatographic separation)。
生产血制品时常见的层析手段如下:
(Wikipedia、《层析技术在血液制品分离纯化中应用的探讨》、财通证券)
亲和层析:将具有特殊结构的亲和分子制成固相吸附剂放置在层析柱中,当要被分离的蛋白混合液通过层析柱时,与吸附剂具有亲和能力的蛋白质就会被吸附而滞留在层析柱中,没有亲和力的蛋白质由于不被吸附,直接流出,从而与被分离的蛋白质分开;该方法将乙醇冷沉淀组分或经DEAE 处理后组分流经偶联有肝素、赖氨酸、明胶等特异性配基的层析柱,使其特异性吸附后,再调整盐浓度及pH 值将其洗脱,适用于获取免疫球蛋白、抗凝血酶及a1-抗胰蛋白酶、a2-巨球蛋白等;
离子交换层析:以离子交换剂为固定相,依据流动相中的组分离子与交换剂上的平衡离子进行可逆交换时的结合力大小的差别而进行分离;该方法将乙醇冷沉组分或血浆经除盐处理后组分以适宜的pH、离子强度、流速流经DEAE、Q、CM 等层析柱,使其吸附或使杂蛋白吸附,从而达到分离目的;适用于获取大多数血液制品组分及去除内毒素;
扩张床层析:将冷冻血浆于常温融化后,按特定流速自下而上流经层析柱,其中杂质及细小碎片直接流穿,随后调节流速、pH、盐浓度,依次洗脱各组分;适用于凝血酶原复合物、凝血因子VIII、VWF、免疫球蛋白、α1-抗胰蛋白酶、白蛋白;
凝胶过滤层析:又称为分子筛层析或体积排阻层析,是利用有一定孔径范围的多孔凝胶作为固定相,对混合物中各组分按分子大小进行分离的层析技术;以较低流速用于分离第一步或最后一步: 前者主要使用G25,用于除盐处理; 后者使用S200或S300,用于蛋白细分或去病毒处理;主要用于获得抗凝血酶、白蛋白等以及去除HAV病毒。
离心/压滤工艺(国元证券)
在生产血液制品的过程中,通常在中间环节中采用离心或者压滤工艺进一步分离沉淀和上清,以加速沉淀的形成。其中,
离心工艺:利用离心机旋转运动的离心力以及物质的沉降系数或浮力密度的差异进行分离、浓缩和提纯
压滤工艺:依靠重力和外界施加的压力,促使悬浮液向特定的方向流动,同时悬浮液内的杂质受到过滤介质的支撑力而被截留,从而分离滤液与杂质,离心工艺具有更高的白蛋白回收率。
三、工艺应用情况
《层析技术在血液制品分离纯化中应用的探讨》
鉴于血制品产业对安全可靠性的要求较高,生产工艺的发展相对稳健,新生产工艺的研发和投入使用周期很长。企业会根据实际需求、监管要求、生产稳定性、投入产出比等诸多因素综合选择生产工艺或多种生产工艺之间的组合。鉴于不同生产工艺的适用范围、安全性、可靠性、生产效率存在一定差异。同一种血液制品可以用多种工艺或工艺组合生产。
白蛋白
人血白蛋白生产可以仅a)单纯采用低温乙醇工艺,也可以b)将低温乙醇工艺搭配层析工艺搭配使用,此外也有海外厂商开发出了无需使用低温乙醇法的c)全层析以及扩张床工艺。低温乙醇工艺将组分V沉淀经过纯化、脱醇、浓缩等环节即可得到人血白蛋白。本文摘录的博雅生物招股书中所列示生产工艺即是单纯使用低温乙醇法生产人血白蛋白的流程。
单纯采用低温乙醇法生产的人血白蛋白产品纯度在90%左右;引入层析供以后,白蛋白纯度可以进一步提升。以CSL研发的生产流程为例,该流程首先使用低温乙醇法分离出组分II+III上清液(不再生产组分V沉淀),经过超滤、除盐、脱乙醇后,使用离子交换层析和凝胶柱层析工艺,可以生产纯度达到99.5%的白蛋白。
上述生产流程仍然涉及使用低温乙醇法作为前道工序;而最新的全层析工艺和扩张床工艺,都已可以直接从血浆分离出最终组分,并具有极高的纯度。同时,因为未使用氢氧化铝吸附,产品中的铝离子含量远低于国际要求水平,安全性更高。
免疫球蛋白
与人血白蛋白类似,球蛋白的生产流程也可分为纯低温乙醇、低温乙醇+层析和不使用低温乙醇的全层析工艺。在使用低温乙醇工艺的生产流程中,免疫球蛋白的制备流程从II沉淀开始,经过溶解、深滤、超滤浓缩等步骤取得免疫球蛋白;卫光生物的球蛋白制备过程既反映了纯低温乙醇法制备免疫球蛋白的流程。使用低温乙醇+层析的方法生产免疫球蛋白的,在生产过程中无需制备组分II沉淀,而是使用层析工艺从组分III上清液开始,经过深层过滤、脱醇、浓缩、层析、配液等环节制程免疫球蛋白。相比之下,扩张床和全层析技术均可不适用低温乙醇,直接制备得到免疫球蛋白,提升产品纯度。
凝血因子
在所有凝血因子类产品中,人纤维蛋白原产品的含量较高,可以使用低温乙醇法获得;其余凝血因子类产品在血浆中的含量较少,常温下化学性质不稳定,难以通过低温乙醇法分离获得。因此,除了人纤维蛋白原以外的凝血因子类产品主要采用层析工艺生产,包括亲和层析、离子交换层析凝胶层析等工艺。博雅生物的生产工艺即反映了使用凝胶、层析等工艺的人凝血酶原复合物及凝血因子VIII的生产流程。
微蛋白
在微蛋白中,采用层析技术制备抗凝血酶、a1-抗胰蛋白酶、a2-巨球蛋白的工艺相对成熟。
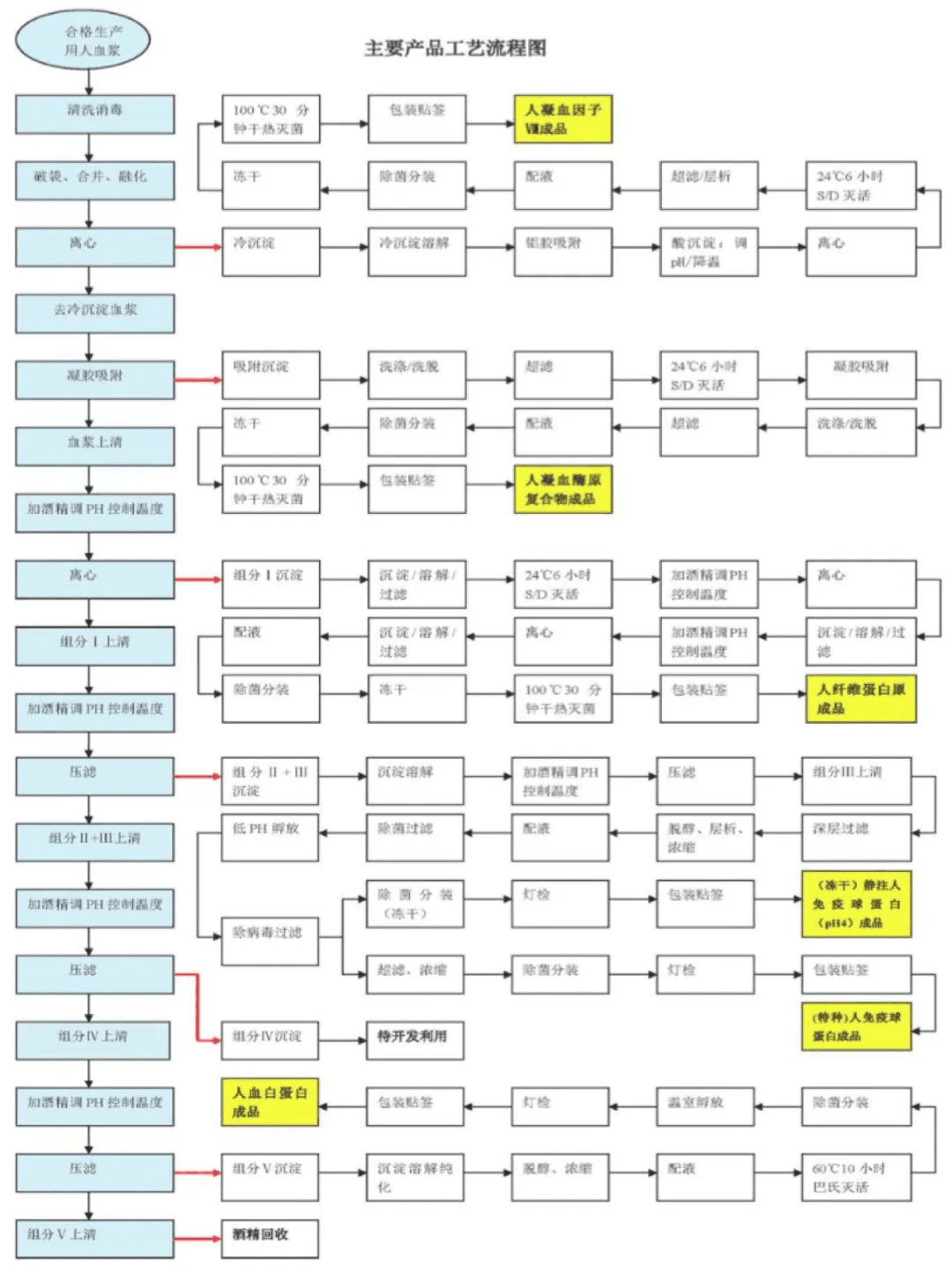
图表 3 - 博雅生物生产工艺流程图
四、国内企业分离提纯工艺发展状况
国内血制品企业的生产工艺仍然存在较大提升空间。一方面,具备规模化生产凝血因子类产品(纤维蛋白原除外)的厂商数量有限;另一方面,大部分厂商仍以低温乙醇法为主生产白蛋白和球蛋白,仅有部分厂商开始使用低温乙醇搭配层析法生产静丙产品。
华兰生物
华兰生物4月22日晚间公告称取得了国家药监局签发的三种规格的静注人免疫球蛋白《临床试验通知书》,上述产品是采用层析纯化工艺和纳米膜过滤+低pH孵放双重去除病毒工艺制备而成的新一代静注人免疫球蛋白,在质量标准、产品收率、病毒安全性等方面均得到了提高,目前国内尚无同类技术及高浓度产品上市。
天坛生物
天坛生物于2020年4月公告了控股子公司成都蓉生投资建设重组凝血八因子车间的公告,总投资4.96亿元;结合其早期公告,成都蓉生的重组因子VIII已经进入临床III期研究阶段,重组因子VIIa处于临床前研究阶段。为了满足重组凝血因子类产品后续的生产需求,成都蓉生拟在永安血制项目基地内新建重组凝血因子生产车间及动物房
天坛生物于2019年12月31日公告称控股子公司成都蓉生药业有限责任公司研制的“静注人免疫球蛋白(pH4、10%)(层析法)”即将开始临床III期试验。根据长江证券的研报,本次天坛生物申报的是采用“全层析法”生产的静丙,回收率超过60%,比低温乙醇法高10%。除了静丙外,其余在研的凝血因子VIII、纤维蛋白原、FIX、重组凝血因子等品种的纯化工艺均采用了层析技术。
博雅生物
博雅生物的静注人免疫球蛋白采用低温乙醇法结合层析工艺生产,每吨血浆可生产静注人免疫球蛋白2600多瓶,位居行业前列。
上海莱士
上海莱士于2017年12月公告称司全资子公司同路生物申请变更工艺,将PEG 沉淀法变更为凝胶吸附结合色谱层析工艺,并已得到国家食品药品监督管理总局批准签发的《药品补充申请批件》。
卫光生物
卫光生物在招股书中披露正在联合北京大学开发结合层析法与沉淀法等蛋白分离纯化技术,从血浆中分离纯化出高纯度、高活性的α1-抗胰蛋白酶等多种血浆蛋白。
双林生物
双林生物官网显示,其发明专利“压滤工艺分离人血浆蛋白的方法”获得中国专利优秀奖、省专利奖金奖、市专利奖金奖。
五、结论
根据公开信息总结,博雅生物的静丙生产工艺较为领先,华兰生物和天坛生物也正在积极研发,短期内对业绩影响有限,但长期看有助于提升公司的综合竞争力。
以上内容建议,仅为天堂硅谷投资管理部研究血制品行业的结论成果,不构成股票推荐的具体建议!